Individualprojekte der KFO 296
Hier finden Sie die Beschreibung der einzelnen Projekte innerhalb der Forschungsgruppe, teilweise mit Videos.
-
Warum unterdrückt Schwangerschaft Schübe der Multiplen Sklerose?
WARUM UNTERDRÜCKT SCHWANGERSCHAFT SCHÜBE DER MS ?
Aktuelle Studien zeigen auf, dass die Immunantwort der Mutter während der Schwangerschaft keinen "immunsuppressiven Zustand" darstellt, sondern eine aktive Anpassung – insbesondere von T-Zellen – an die väterlichen, plazentaren Fremdantigene. Interessante Hinweise auf die übergeordnete Bedeutung dieser Immun-Anpassung kommen aus klinischen Beobachtungen bei Autoimmunkrankheiten, einschließlich Multipler Sklerose (MS). Mehrere Studien haben gezeigt, dass die entzündliche Krankheitsaktivität und das Risiko für sogenannte MS-Schübe während der Schwangerschaft abnehmen, aber nach der Entbindung wieder zunehmen. Die Verringerung der Rückfallrate wird im dritten Trimester auf bis zu 80% geschätzt. Hierbei handelt es sich um eine weitaus höhere Reduktion der Krankheitsaktivität, als bei gegenwärtig verfügbaren MS-Therapien erreicht werden kann. Interessant ist, dass im MS-Mausmodell, der experimentellen autoimmunen Enzephalomyelitis (EAE), trächtige Weibchen ebenfalls vor der Krankheit geschützt sind, nach der Geburt jedoch zunehmende Nervenentzündung aufzeigen.
Das Ziel dieses Projektes ist es, die verantwortlichen Mechanismen zu verstehen, über die durch eine Schwangerschaft herbeigeführte Immunanpassung von Vorteil für den Verlauf der mütterlichen Autoimmunität ist. Basierend auf unseren vorläufigen Daten haben wir die Hypothese aufgestellt, dass die immunologische Anpassung der Mutter an die fetalen Antigenen während der Schwangerschaft auch Auswirkungen auf die Reaktion gegen Körpereigene Antigene hat, wodurch Linderung von Autoimmunerkrankungen eintritt.
Diese Hypothese werden im Tiermodell mit MS-ähnlicher Symptomatik, sowie durch eine klinisch prospektive Kohorte mit weiblichen MS-Patienten im Verlauf der Schwangerschaft und nach der Geburt überprüft.
Innerhalb der Klinischen Forschergruppe 296 steht dieses Projekt in enger Beziehung zu den Projekten „Warum bekommen Frauen ernsthafte Grippeerkrankungen während der Schwangerschaft?“ und „Einfluss von Schwangerschaftshormonen auf die Immunität“, um ein umfassendes Bild von den „Kosten und Nutzen“ des feto-maternalen Immundialoges und den gesundheitlichen Vorteilen und Nachteilen von werdenden Müttern zu erhalten.
/bilder/personen/friese_manuel_202209080001_1_kontaktbild.jpg) Prof. Dr. med.Manuel A. Friese
Prof. Dr. med.Manuel A. Friese- Institutsdirektor
- Facharzt für Neurologie
Kontakt
Standort
Falkenried 94, 20251 Hamburg , Raumnummer 2_63 Prof. Dr.Stefan Gold
Prof. Dr.Stefan Gold- Projektleiter
Kontakt
TelefonTelefaxStandort
Falkenried 94, 20251 Hamburg , 2. Etage, Raumnummer 63 Nina Heckmann
Nina Heckmann- Projektmitarbeiterin
Standort
Falkenried 94, 20251 Hamburg , 2. Etage Dr. rer. Biol. Hum.Caren Ramien
Dr. rer. Biol. Hum.Caren Ramien- Forschungsreferentin
Standort
Hauptgebäude O10 , 2. Etage, Raumnummer 02.2.66.1Dr.Kostas PatasMD- Wissenschaftlicher Mitarbeiter
Standort
S50 Dr. med.Nils Schweingruber
Dr. med.Nils Schweingruber- Assistenzarzt
TelefonE-Mail -
Warum erkranken schwangere Frauen besonders schwer an Grippe?
WARUM ERKRANKEN SCHWANGERE BESONDERS SCHWER AN GRIPPE ?
Schwangere Frauen gehören zu der höchsten Risikogruppe, an Grippe zu erkranken bzw. nach Infektion in die Klinik aufgenommen zu werden. Dieser Nachteil für die Gesundheit von werdenden Müttern wurde besonders deutlich während sogenannter Pandemien, z. B. die kürzlich als mexikanische Grippe oder Schweinegrippe bezeichnete Pandemie im Jahr 2009. Hier hatten mit dem Grippe-Virus infizierte schwangere Frauen ein 5-mal höheres Risiko, in ein Krankenhaus eingeliefert zu werden, als nicht-schwangere Frauen. Deshalb wurden Impfempfehlungen weltweit überarbeitet und die Weltgesundheitsorganisation (WHO) empfiehlt jetzt Impfungen schwangerer Frauen mit höchster Priorität.
Die Mechanismen, die der erhöhten Grippe-Gefahr für schwangere Frauen zugrunde liegen, sind noch weitgehend unbekannt. Deshalb wollen wir verstehen, ob sich das Grippe-Virus verändert, wenn eine schwangere Person damit infiziert ist. Wir wollen außerdem verstehen, wie das mütterliche Immunsystem auf den Grippe-Virus während der Schwangerschaft reagiert und vergleichen dies mit der Immunantwort von nicht schwangeren Personen.
Das Risiko, an einer Grippe während der Schwangerschaft zu erkranken kann durch die Impfung gegen Grippe reduziert, wenn nicht sogar verhindert werden. Überraschenderweise nutzt nur ein kleiner Prozentsatz der Frauen während ihrer fruchtbaren Jahre diese Präventionsmethode. Daher erwarten wir, dass die Erkenntnisse aus unserem Projekt das Bewusstsein bei Frauen während ihrer reproduktiven Jahre verändern und die Impfbereitschaft erhöht.
 Prof. Dr.Gülsah Gabriel
Prof. Dr.Gülsah Gabriel- Projektleiterin
Kontakt
TelefonTelefaxStandort
HPI, 1. Etage, Raumnummer 111 Prof. Dr. med.Petra ArckMD
Prof. Dr. med.Petra ArckMD- Projektleiterin
Standort
Campus Forschung N27 , 4. Etage, Raumnummer 04.039 Standort
Standort
Campus Forschung N27 , 2. Etage, Raumnummer 02.057 Standort
Standort
Campus Forschung N27 , 3. Etage, Raumnummer 03.054Henning JacobsenM. Sc.Standort
HPI, 1. Etage -
Stress während der Schwangerschaft – Folgen für das Kind im späteren Leben?
STRESS UND SCHWANGERSCHAFT – FOLGEN FÜR KIND SPÄTER IM LEBEN
Eine erhöhte Stressbelastung während der Schwangerschaft kann mit Nachteilen für die Gesundheit von Kindern im späteren Leben verknüpft sein, wie zum Beispiel einem erhöhten Risiko für chronische Immunerkrankungen. Hierzu zählen Allergien und Asthma, aber auch Autoimmunerkrankungen wie Multiple Sclerose oder Diabetes. Das Immunsystem entwickelt sich bereits vor der Geburt, daher wird vermutet, dass die Entwicklung der fetalen Immunorgane durch erhöhte Stressbelastungen während der Schwangerschaft gestört werden kann. Die Folge hiervon können das Auftreten von chronischen Immunerkrankungen im späteren Leben des Kindes sein. Trotz der zunehmenden Erkenntnis, dass erhöhte Stressbelastungen während der Schwangerschaft das Risikos für Immunerkrankungen im späteren Leben erhöht, sind die Mechanismen, über welche dieses Risiko vermittelt wird, weitgehend unbekannt. Dies war für uns die Motivation, das vorliegende Projekt zu entwickeln. Wir konzentrieren uns hier auf die Rolle der wichtigsten Stresshormone, den Glukokortikoiden, und deren Einfluss auf die fetale Immun- und Organentwicklung.
Der Fötus benötigt Glukokortikoide, um die strukturelle und funktionelle Entwicklung von Organen wie Lunge oder Immunorgane zu gewährleisten. Überraschenderweise ist der Fötus bis spät in der Schwangerschaft nicht in der Lage, eigene Glukokortikoide zu produzieren. Daher werden mütterliche Glukokortikoide über die Plazenta transportiert, um die fetale Entwicklung zu fördern.
Jedoch muss der Fötus vor zu hohen Spiegeln von mütterlichen Glukokortikoiden geschützt werden, wie sie beispielweise bei erhöhter Stressbelastung produziert werden. Eine Enzym, welches sehr stark in der Plazenta aktiv ist, das sogenannte 11β-Hydroxysteroid-Dehydrogenase Typ 2 (11βHSD-2), steuert normalerweise den Transport von mütterlichen Glukokortikoiden, um den Fötus vor zu hohen Spiegeln von mütterlichen Glukokortikoiden zu schützen.
In Anbetracht der Bedeutung dieses wichtigen Enzyms stellt sich die Frage was passieren würde, wenn 11βHSD-2 in seiner Funktion versagt? Diese Situation könnte eintreten, wenn beispielsweise die Spiegel des Schwangerschaftshormons Progesteron zu niedrig sind.
Wir beabsichtigen, funktionelle Versuche zum besseren Verständnis der Interaktion von Glukokortikoiden, Progesteron und 11βHSD-2 bei Stressbelastung während der Schwangerschaft im Tiermodell durchzuführen, gepaart mit Datenerhebungen von den Studienteilnehmerinnen der Geburtskohorte PRINCE . Dieser Ansatz wird uns erlauben, die Relevanz unserer Erkenntnisse aus Mausmodellen für den Menschen zu verstehen. Wir prüfen, wie Mütter mit hoher Stressbelastung und der damit verbundenen hohen Glukokortikoide-Spiegel im Blut identifiziert werden können. Sobald dies möglich ist, versuchen wir Strategien zu entwickeln, Schwangerschaften frühzeitig zu identifizieren, in welchen das ungeborenen Kind zu hohen Glukokortikoidniveau ausgesetzt ist, um anschließend das Risiko für Immunerkrankungen im späteren Leben zu reduzieren.
WANN ÜBERTRÄGT SICH STRESS AUF DAS UNGEBORENE?
Psychosomatik der Schwangerschaft
Autor: Georg WieghausSTRESS IM MUTTERLEIB
Wie Hormone das Ungeborene beeinflussen
Autorin: Johanna Bayer Prof. Dr. med.Petra ArckMD
Prof. Dr. med.Petra ArckMD- Projektleiterin
Standort
Campus Forschung N27 , 4. Etage, Raumnummer 04.039 Dimitra ZazaraMD
Dimitra ZazaraMD- Nachwuchsgruppenleiterin
- Assistenzärztin in Weiterbildung
- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Klinik und Poliklinik für Geburtshilfe und Pränatalmedizin
- Assistenzärztin in Weiterbildung
Standort
Campus Forschung N27 , 3. Etage, Raumnummer 03.034 -
Schmerzmittel während der Schwangerschaft – ein zweischneidiges Schwert
PARACETAMOL IN DER SCHWANGERSCHAFT: ZWEISCHNEIDIGES SCHWERT
Nur wenige Medikamente können während der Schwangerschaft zur Behandlung von Schmerzen und Fieber verabreicht werden. als sicher angesehen. Das am meisten empfohlene Mittel ist Paracetamol (N-Acetyl-p-aminophenol, Acetaminophen, abgekürzt als APAP). APAP wird seit dem Jahr 1893 verwendet und heutzutage als Medikament zur Behandlung von Schmerzen und Fieber eingesetzt.
APAP ist ohne ärztliche Verschreibungspflicht in der Apotheke erhältlich und wird unter verschiedenen Markennamen, pur oder in Kombination mit anderen Wirkstoffen, wie Vitamin C oder Koffein verkauft. Beginnend in den 1990er Jahren traten in den USA unbeabsichtigte Überdosierungen APAP auf, da die Produktetikettierung nicht eindeutig war, als Folge dieser Überdosierung kam es u.a. zu akutem Leberversagen.
Da APAP in therapeutischen Dosen gut verträglich ist, bleibt es nach wie vor die erste Wahl, um Fieber und Schmerzen während der Schwangerschaft zu behandeln. Warum also beschäftigen wir uns im vorliegenden Projekt mit diesem offensichtlich hilfreichen Medikament?
Aktuelle wissenschaftliche Untersuchungen zeigen, dass APAP auch die Immunantwort verändern kann. Bei Einnahme dieses Medikaments während der Schwangerschaft besteht weiterhin das Risiko, dass es auch zu Veränderungen der Entwicklung des fetalen Immunsystems kommt. Dies kann zu Langzeitfolgen, wie ein erhöhtes Risiko für Asthma und wahrscheinlich auch anderen Autoimmunerkrankungen, im späteren Leben des Kindes führen.
Mit diesem Projekt wollen wir mehr über den Einfluss von APAP während der Schwangerschaft lernen, vor allem, wie genau das Immunsystem von der werdenden Mutter und des ungeborenen Kindes davon beeinträchtigt wird. Es ist noch unbekannt, wie genau APAP mit den sich entwickelnden fetalen Organen interagiert und warum sich daraus langfristigen Folgen entwickeln können.
Wir verfolgen dabei die sogenannt ‚bench-to-bed‘-Strategie, bei welcher wir in Modellen der Grundlagenforschung unter Einbeziehung von Mäusen die komplizierten Prozesse während der Schwangerschaft simulieren. Wir werden sehr sorgfältig die Auswirkungen der APAP und seinen bekannten toxischen Metaboliten N-Acetyl-p-benzochinon (NAPQI) analysieren, speziell im Hinblick auf auftretende Veränderungen der Blutzellen und im Gewebe. Mit High-Tech-Mehrfarben-Durchflusszytometrie wollen wir verschiedene Stammzellen und Immunzellen identifizieren, die mit hoher Wahrscheinlichkeit durch das Medikament beeinflusst werden.
Eine enge Anbindung an die Geburtskohorte PRINCE ermöglicht es uns, die Immunentwicklung des Kindes einzuschätzen und den Einfluss einer Einnahme von APAP während der Schwangerschaft zu bewerten.
Mit den gewonnen Daten und Erkenntnissen wollen wir eine Empfehlung für die Medikation von APAP für Schwangere und ihrer Ärzte ableiten.
Wenn Sie Fragen zu diesem Projekt haben, zögern Sie nicht, sich an uns zu wenden.
RISIKO FÜR EMBRYOS
Ärzte raten Schwangeren von Paracetamol ab
Bericht: Jana Garve Laura Katharina Berkhout
Laura Katharina Berkhout- Doktorandin
TelefonE-Mail -
Pränatale Steroide
PRENATALE STEROIDE
In den letzten 30 Jahren wurden schwangeren Frauen bei einem erhöhten Risiko einer Frühgeburt Kortikosteroide verabreicht, hierzu zählt beispeilsweise Betamethason. Durch dieses Medikament wird die Lungenreifung des ungeborenen Kindes beschleunigen, um die Atmung des möglicherweise zu früh geborenen Kindes zu verbessern. Die deutlich höhere Überlebensrate der Frühgeborenen bestätigt die Wirksamkeit dieser Behandlung. Jedoch wurden langfristige Auswirkungen der Gabe von Betamethason bei drohender Frühgeburt bisher nicht näher untersucht, insbesondere die möglichen Auswirkungen auf das Immunsystem. Hier liegt eine Schädigung durch Betamethason nahe, da bekannt ist, dass Steroids die Entwicklung von T-Zellen stören und den Zelltod herbeiführen können.
Die Entwicklung des Immunsystems von Säugetieren beginnt vor der Geburt. Der Thymus ist ein wesentliches Organ für die T-Zell-Entwicklung und immunologischer Toleranz. Bei der Geburt ist die Thymusfunktion auf ihrem Höhepunkt, somit können Ereignisse, die die Thymusfunktion und Thymusentwicklung vor der Geburt beeinflussen, Folgen für die Immunität des Kindes haben. Die Injektion von physiologischen Dosen von Betamethason im Mausmodell haben eine dramatische Verringerung der Thymusgröße gezeigt, sowie den Zelltod von T -Vorläuferzellen. Anschließend wurde ein beschleunigter Reifungsprozess von T-Zellen beobachtet, welches mit Fehlern in deren Funktion verbunden sein kann. In vitro-Behandlungen von menschlichen Zellen aus dem Thymus, des sogenannten Thymozyten, mit niedrigen Dosen von Betamethason, haben ebenfalls eine Zunahme des Zelltodes bei den sich entwickelnden Zellen gezeigt.
Aktuelle Studien zeigen, dass die Gabe von pränatalen Steroiden ein Risikofaktor für Neugeborene darstellt, an Infektionen kurz nach der Geburt oder an Asthma bzw. Diabetes im späteren Leben zu erkranken. Angesichts der Bedeutung von T-Zellen bei der adaptiven Immunantwort stellen wir die Hypothese auf, dass pränatale Steroidbehandlung die normale Entwicklung des kindlichen Immunsystem beeinträchtigt und das Risiko für Autoreaktivität / Allergie im späteren Leben erhöht.
Der Schwerpunkt unseres Projekts ist die Erforschung der T-Zell-Entwicklung und deren langfristige Auswirkungen auf das Immunsystem – z. B. das Auftreten von Autoimmunität und Allergien – bei Nachkommen, deren Mütter mit pränatalen Kortikosteroiden behandelt wurden.
Da etwa die Hälfte aller Frauen, die mit pränatalen Steroiden bei drohender Frühgeburt behandelt wurden, nicht vorzeitig entbunden haben, könnte das Bewusstsein der schädlichen Langzeitwirkungen für das kindliche Immunsystem zu einer Neubewertung der Behandlungsprotokolle führen.
 Standort
Standort
Campus Forschung N27 , 2. Etage, Raumnummer 02.055 -
Ernährung während der Schwangerschaft und Fettleibigkeit der Mutter – Folgen für das Kind im späteren Leben
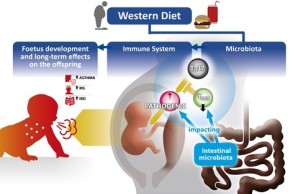
Der Konsum von Nahrungsmitteln mit hohem Zucker-, Fett- und Salzgehalt, häufig als „westliche“ Ernährung bezeichnet, wird derzeit nicht nur in Industrieländern, sondern auch in Entwicklungsländern beobachtet und gilt als eine der Hauptursachen für Fettleibigkeit. Offensichtlich ist eine wachsende Zahl von Menschen aufgrund sozioökonomischer Umstände "gezwungen", diese ungesunde Ernährung zu konsumieren. Im Jahr 2014 litten laut der Weltgesundheitsorganisation 600 Millionen Erwachsene an Fettleibigkeit. Viele von ihnen wurden mit damit assoziierten Stoffwechsel- oder Herz-Kreislauf-Erkrankungen diagnostiziert.
Interessanterweise ist Fettleibigkeit häufig mit chronischen und pathologischen Aktivitäten des Immunsystems verbunden. Epidemiologische Daten weisen zudem darauf hin, dass die westliche Ernährung während der Schwangerschaft und die Fettleibigkeit von Müttern häufig mit chronischen und pathologischen Aktivitäten der Immunentwicklung einhergehen und für die spätere Gesundheit der Kinder verantwortlich sind.Dieses Projekt zielt darauf ab, die zellulären und molekularen Mechanismen dieser Effekte auf die Kindergesundheit aufzuklären. Die Haupthypothese ist, dass die westliche Ernährung und das Übergewicht der Mutter die mütterliche Immunanpassung an die Schwangerschaft beeinflussen, insbesondere die CD4-T-Zellreaktion, die erforderlich ist, um die Toleranz gegenüber dem semi-allogenen Fötus gegenüber Entzündungen zu erhöhen. Diese Entzündung führt wiederum zu einer Beeinträchtigung der fetalen Entwicklung und hat einen entscheidenden Einfluss auf die Zusammensetzung der Darm-Mircrobiota, die wiederum ständig mit dem Immunsystem konfrontiert ist. Wir werden untersuchen, ob die durch Ernährung verursachte Entzündung durch das durch die westliche Ernährung vermittelte Ungleichgewicht der mütterlichen Mikrobiota begründet ist.
Wir verwenden neuartige Multi-Cytokin-Stoffwechselreporter und konditionale Knock-out Mausmodelle, um zu testen, ob die westliche Ernährung von Müttern die Entwicklung des Fötus und die Immunität von Nachkommen über eine veränderte Funktion verschiedener CD4-T-Zell-Untergruppen beeinflusst.
Um die molekularen Details der ernährungsinduzierten Veränderungen in diesen Mäusen zu verstehen, werden wir Einzelzell-Transkriptomik, Epigenetik und modernste computergestützte Ansätze einsetzen. Um zu vergleichen, welche der mechanistischen Erkenntnisse aus den Mausmodellen beim Menschen ähnlich oder unterschiedlich sind, werden Daten und biologische Proben aus der prospektiven Schwangerschaftskohorte PRINCE verwendet. Unser Projekt wird dazu beitragen, neue therapeutische Ziele wie pathogene CD4-T-Zellen zu identifizieren und neue Therapien zu entwickeln, die verhindern sollen, dass Kinder aufgrund der sozialen Umstände, unter denen sie geboren wurden, später unter lebenslangen Gesundheitsproblemen leiden müssen.
Prof. Dr.Nicola Gagliani- Forschungsgruppenleiter
Standort
Campus Forschung N27 , 3. EtageProf. Dr.Stefan Bonn- Institutsdirektor
Standort
Falkenried 94, 20251 Hamburg , Raumnummer 1.58 -
Kongenitale Cytomegalievirus-Infektion
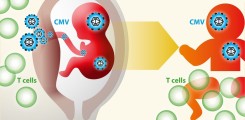
Das Cytomegalievirus (CMV) ist ein großes doppelsträngiges DNS-Virus und Mitglied der Herpesvirus-Familie. Es ist weltweit sehr verbreitet mit einer Seroprävalenz von 40 bis 100%. Die Erstinfektion verläuft bei gesunden Erwachsenen meist subklinisch, da das Immunsystem die Virusvermehrung bekämpfen kann. Insbesondere die T-Lymphozyten sind bekannt dafür, einen essentiellen Beitrag zur Kontrolle der CMV-Infektion zu leisten. Dennoch kann diese antivirale Immunantwort das Virus weder auslöschen noch eine Superinfektion mit zusätzlichen CMV-Stämmen oder die Reaktivierung einer latenten Infektion verlässlich verhindern.
Die kongenitale CMV-Infektion bei Neugeborenen ist die häufigste Ursache für dauerhafte Behinderungen wie beispielsweise ein sensorineuraler Hörverlust oder geistige Entwicklungsstörungen. Ungefähr 1% der Kinder weltweit werden mit einer CMV-Infektion geboren. Davon sind ca. 10% klinisch symptomatisch bei Geburt und werden wahrscheinlich langfristig an Folgeerkrankungen leiden. Weitere 5-10% der Kinder entwickeln eine Behinderung erst später.
Welche Faktoren zur vertikalen Übertragung des Virus von Mutter zum Fötus und zur einer CMV-Erkrankung führen, bleiben bis jetzt unbekannt. Hinzu kommt, dass derzeit kein Impfstoff verfügbar ist, und die einzige mögliche Behandlung mit Valganciclovir ist mit dem Risiko schwerer Nebenwirkungen verbunden.
In diesem Projekt haben wir das Ziel, Faktoren zu definieren, die das Risiko einer kongenitalen CMV-Infektion sowie einen schweren Verlauf der Krankheit erhöhen. Wir werden die Rolle von pränatalen Stressfaktoren bestimmen, ebenso die anti-CMV-T-Zell-Antwort von Mutter und Kind sowie virale Pathogenitätsfaktoren. Wir untersuchen, ob mütterlicher Stress oder Medikamenteneinnahme während der Schwangerschaft das Kind anfälliger für einen schweren Verlauf einer CMV-Infektion im frühen Lebensalter macht. Beides sind potenziell vermeidbare Stressfaktoren. Die detaillierte Charakterisierung mütterlicher und kindlicher T-Zellen wird Einblick in deren Rolle bei der Bekämpfung von CMV-Infektionen während der frühen Lebenszeit geben. Abschließend untersuchen wir den Erreger selbst, um virale genetische Faktoren zu identifizieren, die seine Pathogenität und die Wahrscheinlichkeit der Mutter-zu-Kind Übertragung erhöhen. Zusammenfassend wollen wir diese dringenden offenen Fragen zur CMV-Infektionsbiologie beantworten, um damit die Grundlage für neue diagnostische oder therapeutische Ansätze zu bilden.
Prof. Dr. Wolfram Brune
Leiter der Forschungsabteilung Virus-Wirt-Interaktion
Heinrich-Pette-Institut
Leibniz-Institut für Experimentelle Virologie
Martinistraße 52
20251 HamburgE-Mail wolfram.brune@leibniz-hpi.de
 Prof. Dr. med.Felix StahlPhD
Prof. Dr. med.Felix StahlPhD- Facharzt
- Wissenschaftlicher Arbeitsgruppenleiter
- Facharzt für Laboratoriumsmedizin
Kontakt
TelefonTelefaxMobilE-MailStandort
Campus Forschung N27 , 2. Etage, Raumnummer 02.054 -
PRINCE-Studie – Prospektive Geburtenkohortenstudie „Pränatal bestimmende Faktoren bei der Gesundheit von Kindern"
PRINCE-STUDIE
Die Weichen für einen guten Start ins Leben werden schon vor der Geburt gestellt. Im Rahmen der PRINCE-Studie (Prenatal Identification of Children’s Health) wollen wir genauer untersuchen, welche Faktoren während der Schwangerschaft einen Einfluss auf die lebenslange …
Wann überträgt sich Stress auf das Ungeborene?
Psychosomatik der Schwangerschaft
Autor: Georg WieghausStress im Mutterleib
Wie Hormone das Ungeborene beeinflussen
Autorin: Johanna BayerKlinische Leitung der PRINCE-Studie
 Prof. Dr. med.Anke Diemert
Prof. Dr. med.Anke Diemert- Oberärztin
- Fachärztin für Frauenheilkunde und Geburtshilfe
- Spezielle Geburtshilfe und Perinatalmedizin
- DEGUM II
Kontakt
TelefonTelefaxMobilE-MailStandort
Hauptgebäude O10 , 2. EtageKontakt
 Prof. Dr. med.Petra ArckMD
Prof. Dr. med.Petra ArckMD- Projektleiterin
Standort
Campus Forschung N27 , 4. Etage, Raumnummer 04.039 Prof. Dr. med.Kurt Hecher
Prof. Dr. med.Kurt Hecher- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Klinik und Poliklinik für Geburtshilfe und Pränatalmedizin
- Facharzt für Frauenheilkunde und Geburtshilfe
- Spezielle Geburtshilfe und Perinatalmedizin
- DEGUM III
Kontakt
TelefonTelefaxE-MailStandort
Hauptgebäude O10 , 4. Etage Univ.-Prof. Dr. med.Ania C. Muntau
Univ.-Prof. Dr. med.Ania C. Muntau- Klinikdirektorin
- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Klinik und Poliklinik für Kinder- und Jugendmedizin
- Fachärztin für Kinder- und Jugendmedizin
Standort
O45 , 1. Etage, Raumnummer 01.5.014.1 Prof. Dr. med.Dominique Singer
Prof. Dr. med.Dominique Singer- Ärztlicher Leiter
- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Sektion Neonatologie und Pädiatrische Intensivmedizin
- Facharzt für Physiologie
- Facharzt für Kinder- und Jugendmedizin
- Spezielle Pädiatrische Intensivmedizin
- Neonatologie
Standort
O45 , 1. Etage Prof. Dr.Eva Tolosa
Prof. Dr.Eva Tolosa- Forschungsgruppenleiterin
- Projektleiterin
Standort
Campus Forschung N27 , 2. Etage, Raumnummer 02.055 Dr. med.Corinna Kramer
Dr. med.Corinna Kramer- Ärztin
- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Klinik und Poliklinik für Geburtshilfe und Pränatalmedizin
Standort
O45 , EG, Raumnummer 00.5.012.1 Dr. med.Mirja Pagenkemper
Dr. med.Mirja Pagenkemper- Projektmitarbeiterin
- Zentrum für Geburtshilfe, Kinder- und Jugendmedizin
- Klinik und Poliklinik für Geburtshilfe und Pränatalmedizin
- Fachärztin für Frauenheilkunde und Geburtshilfe
Standort
Hauptgebäude O10 , 5. Etage Gudula HansenM. Sc. Health Services Management
Gudula HansenM. Sc. Health Services Management- Ernährungsberaterin
Kontakt
TelefonTelefaxMobilE-MailStandort
Hauptgebäude O10 , 2. Etage, Raumnummer 02.8.076.1