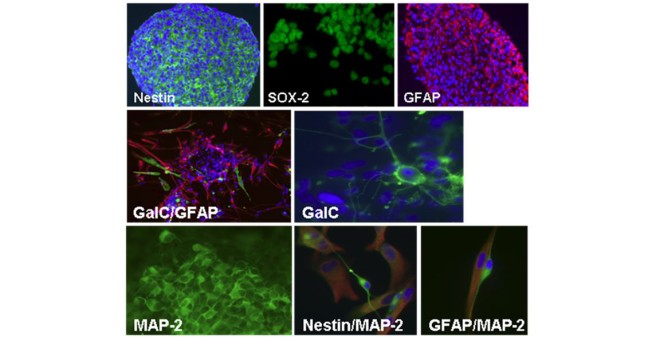
Abb. 1 Expression von Stamm- bzw. Vorläuferzellantigenen durch die Glioblastomstammzelllinien (Nestin, SOX-2) unter Stammzellkulturbedingungen. Expression des astrozytären Markers GFAP vor und nach Andifferenzierung der Zellen sowie Expression des oligodendroglialen Markers GalC und des neuronalen Markers MAP-2 nach Andifferenzierung der Zellen.
Tumorstammzellen
Glioblastome entwickeln sich aus einer einzelnen Zelle, die durch verschiedene Mutationen entartet ist. Man nimmt an, dass die Teilung dieser ersten Tumorstammzelle asymmetrisch verläuft, d.h., dass eine der beiden entstehenden Tochterzellen wiederum Tumorstammzelleigenschaften hat, die andere hingegen einen differenzierteren Phänotyp aufweist. Auch die weiteren Teilungen der Tumorstammzellen verlaufen jeweils asymmetrisch, so dass sich die Tumorstammzellen fortwährend selbsterneuern. Zu den Eigenschaften der Tumorstammzellen gehören neben der Selbsterneuerungskapazität vor allem die Fähigkeit zur Initiierung von Tumoren in vivo (hierzu gehört auch die Absiedelungsfähigkeit in andere Regionen oder Organsysteme 1,2), die Expression von stammzelltypischen Markern sowie die Multipotenz (bei Gliomen: astrozytäre, oligodendrogliale und neuronale Differenzierbarkeit). Tumorzellen mit Stammzelleigenschaften machen nur einen geringen Prozentsatz aller Tumorzellen aus, sind jedoch entscheidend für den kontinuierlichen Erhalt des Tumors verantwortlich. Differenziertere Tumorzellen bilden die Hauptmasse des Tumors und können sich ebenfalls noch teilen, aber vermutlich nur wenige Male und nicht unbegrenzt. Darüberhinaus sind Tumorstammzellen im Gegensatz zu den differenzierteren Zellen sehr viel therapieresistenter. Es wird angenommen, dass Tumorrezidive nach Chemo- oder Strahlentherapie von verbliebenen Tumorstammzellen ausgehen, weshalb die Tumorstammzellen das eigentliche Hauptziel der Therapie sein müssen. In vorangegangenen Arbeiten etablierten wir mehr als 30 Glioblastomstammzelllinien durch Kultivierung von Zellen unter neuralen Stammzellkulturbedingungen und charakterisierten diese Linien in vitro und in vivo (3,4,5,6,7). Die Zelllinien wachsen sphärisch, exprimieren stammzelltypische Antigene, lassen sich in neuronale, astrozytäre und oligodendrogliale Richtung differenzieren, sind kontinuierlich teilungsaktiv, bilden als Klone neue Subsphären und wachsen im Hirn von Mäusen überwiegend diffus invasiv.
Durch Modifikation der Stammzellkulturbedingungen ließen sich darüberhinaus, isogene Paare von Zelllinien aus einzelnen Glioblastomen kultivieren, von denen jeweils eine Zelllinie eine (im Ursprungstumor vorhandene) Amplifikation des Epidermal Growth Factor Rezeptors (EGFR) beibehalten hat, wohingegen die Amplifikation in der anderen Zelllinie fehlt6. Außerdem gelang es durch diese optimierten Zellkulturbedingungen auch, Zelllinien zu generieren, welche die Expression der konstitutiv aktiven Rezeptordeletionsvariante EGFRvIII beibehalten haben. Diese Paare von Zelllinien sind ein Modell für die im Tumor vorhandene zelluläre Heterogenität und ermöglichen vergleichende Analysen zum Ansprechen von Glioblastomzellen mit unterschiedlichem EGFR Status auf Chemo- und Strahlentherapie sowie auf speziell gegen den EGFR gerichtete Therapeutika ( vgl. Webseite zum EGFR ). Durch Genexpressionsanalysen an kultivierten Glioblastomzelllinien sowie Glioblastomgeweben ließ sich eine Gruppe von Glioblastomstammzelllinien identifizieren, deren Genexpressionsprofile besonders stark denen humaner Glioblastome gleichen. Diese Zelllinien zeigen zudem eine besonders starke Ausprägung von Tumorstammzelleigenschaften. Die transkriptionelle Ähnlichkeit kultivierter Zelllinien mit Originaltumoren ist demzufolge mit einem unterschiedlichen Ausprägungsgrad an Stammzelleigenschaften assoziiert. Unter den Genen, die besonders hoch sowohl in Glioblastomen als auch in Zelllinien mit besonders intensiv ausgeprägten Stammzelleigenschaften exprimiert sind, ist das CXCR4 Gen, welches für den Rezeptor des Zytokins Stromal Cell Derived Factor-1 (SDF-1) kodiert. In Glioblastomstammzelllinien exprimiert nur eine Subpopulation der Zellen den CXCR4 Rezeptor (ca. 10-15%), und diese Subpopulation ist teilidentisch mit einer Subpopulation, die den Tumorstammzellmarker CD133 exprimiert, was dafür spricht, dass CXCR4 ebenfalls ein Tumorstammzellmarker ist. Diese CXCR4 und CD133 positive Subpopulation lässt sich durch Hypoxie expandieren. Da der CXCR4 Rezeptor im normalen erwachsenen Hirngewebe kaum exprimiert wird, ist er ein potenziell vielversprechendes Target zur selektiven Hemmung des Wachstums von Glioblastomstammzellen. AMD3100 ist ein spezifischer CXCR4 Antagonist, dessen Wirkung wir in einem Glioblastomstammzell-Xenotransplantatmodell in Mäusen untersuchten. Die Behandlung der Mäuse mit AMD3100 reduzierte das Tumorwachstum um ca. 60% gegenüber Kontrollen. Demzufolge erscheint eine multimodale therapeutische Strategie sinnvoll, bei der nach Operation eines Glioblastoms die verbleibenden Tumorzellen einerseits mit Chemo-und/oder Strahlentherapie zerstört werden und zusätzlich die Tumorstammzellkomponente, welche überwiegend in hypoxischen Nischen lokalisiert ist, durch Antagonisierung von CXCR4 angegriffen wird. Erkenntnisse der vergangenen Jahre sprechen zunehmend dafür, dass Tumorstammzellen keine fixe, unveränderliche Zellsubpopulation sind, sondern dass auch nicht-Tumorstammzellen in der Lage sind, Stammzelleigenschaften wie z.B. die Tumorinitiierungsfährigkeit zu aquirieren. Hierbei spielen veränderliche Faktoren des Mikromilieus eine große Rolle. Ein wesentlicher solche Faktor ist die Gewebshypoxie, d.h. die geringe Sauerstoffkonzentration im Tumorgewebe, die regional sogar unter 0.1% liegen kann. Hypoxie fördert die Ausprägung von Stammzelleigenschaften bei Tumorzellen, und es wird angenommen, dass Tumorstammzellen im Gewebe vor allem in hypoxischen Nischen lokalisiert sind. Die Sauerstoffkonzentrationen im Tumorgewebe fluktuieren während der Tumorprogression in verschiedenen Regionen erheblich, abhängig von Parametern wie Zelldichte, Gewebsdiffusion, Nekrosen und der Entstehung neuer Blutgefäßen (Angiogenese). Diesen schwankenden Sauerstoffkonzentrationen müssen sich die Tumorzellen anpassen können, um zu überleben. Man nimmt an, dass insbesondere die Tumorstammzellen eine besonders hohe metabolische Flexibilität besitzen, durch die sie ihren Metabolismus z.B. von verstärkter oxidativer Phosphorylierung zu verstärkter Glykolyse regulatorisch verschieben können und sich so an Veränderungen der Mikorumgebung adaptieren können. Diesem metabolischen Adaptationsmodell zufolge besteht das Problem einer effizienten Tumortherapie nicht darin, eine minimale Subpopulation von Tumorstammzellen zu vernichten, sondern darin zu verhindern, dass Tumorzellen sich immer wieder erneut ihrer Mikroumgebung durch Aktivierung verschiedener Überlebens-Pathways anpassen können. Um metabolische Adaptationsmechanismen zu identifizieren untersuchten wir Veränderungen der Genexpression in Glioblastomstammzelllinien bei akuter und chronischer Hypoxie sowie akuter und chronischer (Hyper-)Oxygenierung. Hierbei zeigte sich, dass die Tumorzellen bei hoher Sauerstoffkonzentration eine relativ hohe Aktivierung des Pentosephosphatweges haben, wohingegen es bei akuter Hypoxie zu einem metabolischen Switch hin zu verstärkter Glykolyse kommt7. Hiermit einhergehend vermindern die Tumorzellen bei akuter Hypoxie ihre Proliferation, aber steigern die Migration, vermutlich als kompensatorischen Mechanismus, welcher im Tumor dazu dient, Gewebsarealen mit akutem hypoxischem Stress zu entkommen (vgl. Webpage zum Tumormetabolismus ).