Die schleichende Pandemie stoppen
UKE-Forschende haben sich Röntgenquellen aus dem Bahrenfelder Deutschen Elektronen-Synchrotron (DESY) zunutze gemacht, um erstmals zu sehen, wie Bakterien Antibiotika unschädlich machen. Ein Schlüssel für neue Waffen im Kampf gegen Antibiotikaresistenzen?
Von Sandra Wilsdorf
Mehr als eine Million Menschen sterben weltweit jedes Jahr an Infektionskrankheiten, weil kein Antibiotikum ihnen helfen konnte. Und es werden immer mehr: „Das ist eine schleichende Pandemie“, sagt Prof. Dr. Martin Aepfelbacher, Direktor des Instituts für Medizinische Mikrobiologie, Virologie und Hygiene des UKE. Neue Waffen gegen antibiotikaresistente Erreger zu entwickeln, ist deshalb eine der dringlichsten Aufgaben moderner Medizin. Aepfelbacher und Kolleg:innen sind dabei möglicherweise wesentliche Schritte weitergekommen: Gemeinsam mit Prof. Dr. Christian Betzel, Leiter des Instituts für Biochemie und Molekularbiologie der Universität Hamburg, sowie Kolleg:innen der Science City Bahrenfeld konnten sie im Rahmen des von der Joachim Herz Stiftung geförderten Forschungskonsortiums Infectophysics erstmals einen der medizinisch bedeutsamsten Resistenzmechanismen sehen und so verstehen, wie genau er funktioniert.
Bei einer Resistenzentwicklung gelingt es Bakterien, mit Hilfe sogenannter Betalaktamasen gängige Substanzen aus der Gruppe der Betalaktam-Antibiotika wie Penicilline und Cephalosporine zu zerstören, noch bevor diese den Erreger abtöten können. Zwar wurden inzwischen Medikamente entwickelt, die die Betalaktamasen hemmen und so dem Antibiotikum zu seiner Wirkung verhelfen sollen – sogenannte Betalaktamase-Inhibitoren. Doch auch diese werden zunehmend weniger wirksam. Denn Bakterien haben ihrerseits Mutationen an den Betalaktamasen entwickelt, die die Bindung des Inhibitors reduzieren oder verhindern. „Es ist eine Art Hochrüsten, das wir jetzt durchbrechen wollen“, sagt Aepfelbacher.



Film aus der Zelle
Die Forscher:innen haben jetzt die Grundlagen für eine strukturbasierte Weiterentwicklung der Betalaktamase-Inhibitoren gelegt. Der Schlüssel: das Verständnis der exakten Mechanismen. „Man weiß tatsächlich nicht in ausreichender Präzision, wie genau ein Betalaktam-Antibiotikum von einer Betalaktamase gespalten wird. Aber natürlich können wir nur dann intelligente Lösungswege finden, wenn wir diesen Reaktionsmechanismus genau kennen“, erklärt Prof. Dr. Holger Rohde, Oberarzt und Forschungsgruppenleiter im Institut für Medizinische Mikrobiologie, Virologie und Hygiene.
Ermöglicht hat diese Einblicke unter anderem die besonders helle und deshalb brillante Röntgenquelle PETRA III und der „EuropeanXFEL“ auf dem DESY-Campus, einer der modernsten Röntgenlaser der Welt. Er erzeugt ultrakurze Laserlichtblitze im Röntgenbereich – 27 000 Mal in der Sekunde und milliardenfach intensiver als die der besten herkömmlichen Röntgenquellen. „Damit konnten wir nicht nur, wie bisher, eine chemische Reaktion zu einem bestimmten Zeitpunkt sehen, sondern die Dynamik der Prozesse im Millisekundenbereich“, erklärt Rohde.



Der Schneidemechanismus
Und diese sichtbar gemachten Prozesse zeigen, wie die Betalaktamase das Antibiotikum zerstört. Dabei funktioniert das Enzym wie eine Art molekulare Schere, es zerschneidet die sogenannten Laktam-Ringe der Antibiotika und macht sie so wirkungslos. Die zusätzlich verabreichten Inhibitoren, die genau das verhindern sollen, legen sich bildlich gesprochen zwischen die Scherenblätter des Enzyms und blockieren die Schneidefunktion. Durch Mutationen kann sich jedoch wiederum die Form der molekularen Schere ändern. Auch diesen Prozess konnten die Wissenschaftler:innen zum ersten Mal sehen. „Wir verstehen jetzt besser, wie die Schere funktioniert und wie sie blockiert werden kann“, sagt Rohde. In einem nächsten Schritt probierten sie genau das mit einem Medikament aus, das aktuell in der Tumortherapie eingesetzt wird und von dem vermutet wurde, dass der Wirkstoff auch ein Betalaktamase-Inhibitor sein könnte. Dank des Röntgenlasers konnte das nun bestätigt und zudem der zugrundeliegende Mechanismus dargestellt werden.
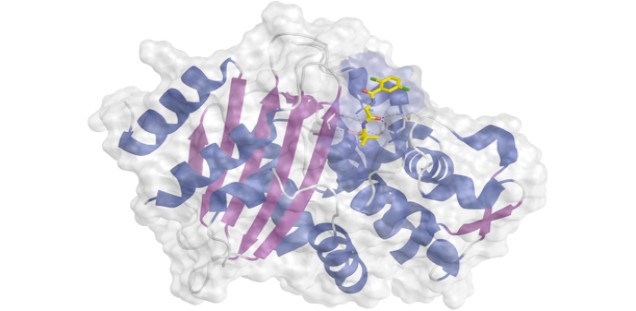
Bild nachfolgend:
Das Enzym Betalaktamase zerschneidet ein Antibiotikum und macht es unwirksam
Die Hoffnung: Grundlage für etwas Neues
Aus diesen in dem hamburgweiten interdisziplinären Forschungsprojekt Infectophysics gewonnenen Erkenntnissen etwas zu entwickeln, das künftig Einsatz in der Medizin findet, liegt nun in anderen Händen. Dafür wollen die Forschenden ihre Ergebnisse breit und international publizieren. „Wir hoffen, dass andere Forschende den nächsten Schritt gehen oder die Pharmaindustrie daraus etwas entwickelt“, sagt Prof. Aepfelbacher. Und natürlich, so der Mikrobiologe, fließen die Erkenntnisse aus Infectophysics auch im UKE in weitere Projekte ein.
Mehr Informationen?
Details zu allen Projekten des Forschungsprojekts gibt es hier: www.uke.de/infectophysics
Vorheriger Beitrag:
Männer erkranken anders. Frauen auch.
Nächster Beitrag:
Schalter gegen Alzheimer
Übersichtseite
Zurück zur Übersicht